엔케이맥스"난치성 육종암 환자의 종양 78% 사멸"
[서울경제TV=김혜영기자]엔케이맥스는 미국 FDA 동정적 사용 제도 승인을 받은 슈퍼NK(SNK01)와 키트루다(Keytruda) 병용요법 치료 환자에게서 긍정적인 결과를 얻었다고 23일 밝혔다.
이번에 공개된 데이터는 육종암의 일종인 결합조직성소원형세포종(DSRCT) 환자에 대한 슈퍼NK+키트루다의 동정적 사용으로 투여 받은 환자의 임상 결과이다. 해당 환자는 2017년 육종암을 판정 받은 32세의 남성 환자로 약 1년 반 동안 기존 화학요법으로 치료를 진행했으나 암세포가 줄어들지 않고 독성(toxicity)이 나타났다. 이후 키트루다 약물을 추가로 투여 받았지만 계속해서 암이 커지는 PD(progression disease)를 보여 16싸이클(cycle)에 치료가 중단됐던 상태였다.
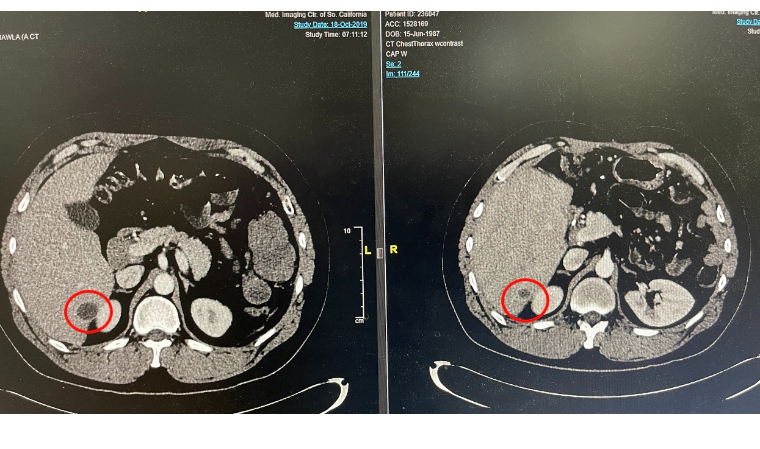
이후 이 환자는 동정적 사용 환자로 등록되어 2년간 슈퍼NK와 키트루다 병용 투여를 받았다. 그 결과, 간문에 있던 종양의 크기가 61 X 35mm에서 35 X 30mm로 줄어들었고 간에 퍼져 있던 종양의 크기가 51 x 37 mm에서 16 x 7 mm로 줄었다. 이로써 2019년부터 2021년 11월 현재까지 간에 발생한 암의 약 78%가 사멸하는 결과를 보였다고 회사측은 설명했다.
동정적 사용(Compassionate Use)은 암과 같이 생명을 위협하고 장기간 또는 중증 질환의 적절한 치료 대안이 없을 때 개발 중이나 아직 판매허가를 취득하지 못한 신약 치료제의 사용을 승인하여 치료의 기회를 주는 FDA 제도이다.
이번 동정적 사용제도로 치료받은 환자의 담당의인 차울라(Chawla) 박사는 “전이성 말기 육종암 환자들에게서 SNK01과 면역관문억제제의 병용요법에 치료효과를 보인 것은 굉장히 놀라운 일"이라며 "더군다나 이들은 기존 4~5차 이상의 화학치료에 실패한 환자들이다”고 말했다. 그는 이어 “특히 동정적 사용을 통해 치료를 진행한 DSRCT 환자의 경우 2년동안의 장기간 투여에도 부작용이 전혀 없었으며, 현재 계속적인 투여를 받으며 정상적인 생활을 하고 있다”며 “이러한 결과는 추후 육종암에 대한 희귀의약품 개발 및 허가에 중요한 지표가 될 수 있다”고 밝혔다
박상우 엔케이맥스 대표는 “이번 동정적 사용 데이터를 통해 약물의 우수성 확인은 물론 FDA의 희귀의약품 지정(Orphan Drug Designation) 과정에서도 매우 귀중한 자료로 사용될 수 있을 것으로 기대한다”며 “현재 진행 중인 육종암 임상 성공적인 완료와 함께 미충족 의료수요가 높은 육종암 분야에서 가장 먼저 FDA허가 및 상용화를 목표로 개발에 박차를 가할 계획”이라고 말했다./hyk@seadaily.com
[ⓒ 서울경제TV(www.sentv.co.kr), 무단 전재 및 재배포 금지]

관련뉴스
- 강태영 농협은행장 "초개인화·생산적 금융·Agentic AI로 전략 전환"
- 김인 새마을금고중앙회장 "리스크 관리가 곧 조직 생존"
- 이창용 “고환율 기대 관리…연초 외환시장 경계”
- 병오년 증시 ‘활짝’…새해 첫날 쌍끌이 랠리
- "디지털 자산·AI 시장 선점... 4대금융 '대전환' 선언
- 박상진 산업은행 회장 "올해가 국가 경제·산은 성장 골든타임"
- 양종희 KB금융 회장 "전환과 확장 통해 미래 성장 기반 구축"
- 윤의수 전 신협 대외협력이사 "신협 위기, 개별 조합 아닌 구조 문제"…중앙회장 도전장
- [부고] 강진두(KB증권 대표이사)씨 모친상
- 정일선 광주은행장 취임…"지역금융 새 기준 제시할 것"
주요뉴스
기획/취재
주간 TOP뉴스
- 1명현관 해남군수 "2026년, 해남이 대한민국 AI·에너지 수도 심장 될 것"
- 2김한종 장성군수 "화합의 ‘대동 장성’으로 재도약"
- 3새고창로타리클럽, 고창군에 이웃돕기성금 300만 원 기탁
- 4말보다 현장, 협치로 답하다…장수군의회 2025 의정 결산
- 5강태영 농협은행장 "초개인화·생산적 금융·Agentic AI로 전략 전환"
- 6김인 새마을금고중앙회장 "리스크 관리가 곧 조직 생존"
- 7양주시, ‘대한민국 새단장’ 최우수…특별교부세 1억 확보
- 8포천시, 주택행정 평가 장려상
- 9김동연 지사, 일산대교 현장 방문… 전면 무료화 추진 재확인
- 10이상익 함평군수, 2026년 청렴 서약…“신뢰받는 함평 구현 앞장”
































댓글
(0)